Plan de cours
consigne : à faire en classe
- Cours (lire et comprendre) : livre §1 et §3 p.142
- Activité (à faire) : livre 3 p.140
- Exercices (à faire) 13p.146, 14p.146, 20p.147, 24p.148, 22 p.205
Devoirs à la maison
- Cours et vocabulaire à apprendre (recopier ou résumer)
- Visualiser les activités complémentaires PCCL
- Applications vérification et utilisation des connaissances
Exercices 1,2,3,4,13,14,20,24 p.144 et 22 p.205
Cours et vocabulaire
§1 p.142
Un ion est un atome ou une molécule qui a gagné ou perdu un ou plusieurs électrons.
L’ajout (le gain) d’un ou plusieurs électrons donne un ion négatif : un anion. Par exemple, l’atome de chlore Cl gagne un électron pour devenir l’ion chlorure Cl−.
La perte d’un ou plusieurs électrons donne un ion positif : un cation. Par exemple, l’atome de cuivre Cu perd deux électrons pour devenir l’ion cuivre Cu2+.
§3 p.142
Un solide ionique est un assemblage régulier d’anions et de cations. Par exemple des cristaux de sels sont composés d’autant d’ions Na+ que d’ions Cl−.
Une solution ionique est une solution de cations et d’anions, le plus souvent aqueuse. Sa formule s’écrit entre parenthèses avec les formules des ions qu’elle contient. Par exemple, la solution de chlorure de fer s’écrit (Fe3+ + 3 Cl–).
Les solides et les solutions ioniques sont électriquement neutres.

| Vocabulaire | Définition |
| ion | formé à partir d’un atome ou d’une molécule ayant gagné ou perdu un ou plusieurs électrons |
| anion | ion ayant gagné un ou plusieurs électrons. |
| cation | ion ayant perdu un ou plusieurs électrons. |
| ionique | adjectif : qui contient des ions une solution ionique est un liquide contenant des ions |
| aqueuse | adjectif : qui est à base d’eau une solution dont le solvant est l’eau |
Livre
Activités pour comprendre
Activité 3 p.140 Des composés ioniques qui soignent
Livre

Corrigé
1) ion sodium : Na+ est un cation ; ion ferrique : Fe3+ est un cation ; ion chlorure : Cl– est un anion.
2.a) On trouve 1 ion sodium pour 1 ion chlorure. D’après sa formule (Na+ + Cl– ), le chlorure de sodium est composé d’un ion sodium par ion chlorure présent.
2.b) Le mélange des 2 ions n’est pas chargé ; il est neutre, autant de charges + que de charges –
2.c) La charge de l’ion Fe3+ est trois fois plus grande que la charge de l’ion Cl–
2.d) Afin d’obtenir une solution électriquement neutre, le chlorure ferrique doit contenir trois fois plus d’ions chlorures Cl– que d’ions ferriques Fe3+
3) La formule chimique du chlorure ferrique est ( 1 Fe3+ + 3 Cl– )
activités complémentaire
activités PCCL
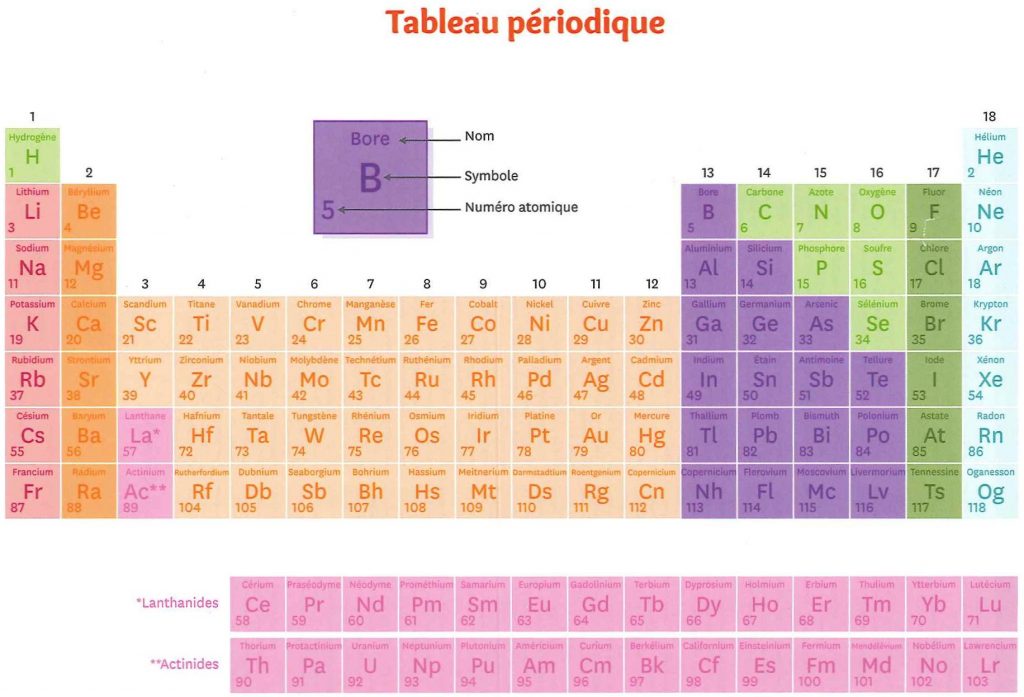
tableau périodique
Applications vérification des connaissances
exercices 1,2,3,4,13,14 p.144>
utilisation des connaissances
exercices 20,24 p.144 et 22 p.205 >
CDT
3e Matière 6 : Ion – électriquement chargé
https://cours.saettler.org/3m6/
Cours : livre p.142
Activité : livre 3 p.140
Exercices : livre 13p.146, 14p.146, 20p.147, 24p.148, 22 p.205
Programme : M2.6 Associer leurs symboles aux éléments à l’aide de la classification périodique» Dioxygène, dihydrogène, diazote, eau, dioxyde de carbone.
Devoirs
https://cours.saettler.org/3m6/
Retravailler le cours, les activités, les exercices
Apprendre le cours et le vocabulaire (recopier ou résumer)
Visualiser les activités complémentaires PCCL
Faire les exercices : Applications vérification et utilisation des connaissance 1,2,3,4,13,14,20,24 p.144 et 22 p.205
Devoirs préparatoire au TP
étudier le document, visualiser la vidéo et la fiche méthode
dessiner le schéma d’un test de reconnaissance
étudier le document : https://www.pccl.fr/physique_chimie_college_lycee/troisieme/cours_exercices_corriges/ions_pH.htm
visualiser la vidéo : https://www.youtube.com/watch?v=02LffwR95Gs
et la fiche méthode : https://cours.saettler.org/wp-content/uploads/2018/07/Test-de-reconnaissance-des-ions.jpg


