Consignes de travail
Avant le cours – préparation :
Compléter la fiche de travail à l’aide de la partie Cours et vocabulaire.
Faire les exercices Application – vérification des connaissances, et compléter la fiche de travail.
Étudier les Activités complémentaires (vidéos, liens, autres fiches,…).
Identifier les questions à poser lors du cours.
Pendant le cours – compréhension :
Poser les questions identifiées lors de la préparation du cours.
Faire les activités restantes proposées.
Après le cours – apprentissage :
Apprendre par cœur le Cours et vocabulaire.
Terminer toutes les activités et exercices d’application.
Livre
Cours et vocabulaire

à la maison
Il existe deux versions de la charge électrique : l’une positive, l’autre négative. Les charges de mêmes signes se repoussent, celles de signes opposés s’attirent.
Les atomes sont formés de protons chargés positivement, de neutrons électriquement neutres et d’électrons chargés négativement. Les protons et les neutrons, appelés nucléons, forment le noyau. Les électrons sont en mouvement autour du noyau, ils forment le nuage électronique. L’atome est électriquement neutre, il comporte autant de protons que d’électrons, sa charge électrique totale est nulle. Le numéro atomique Z est le nombre de protons du noyau.
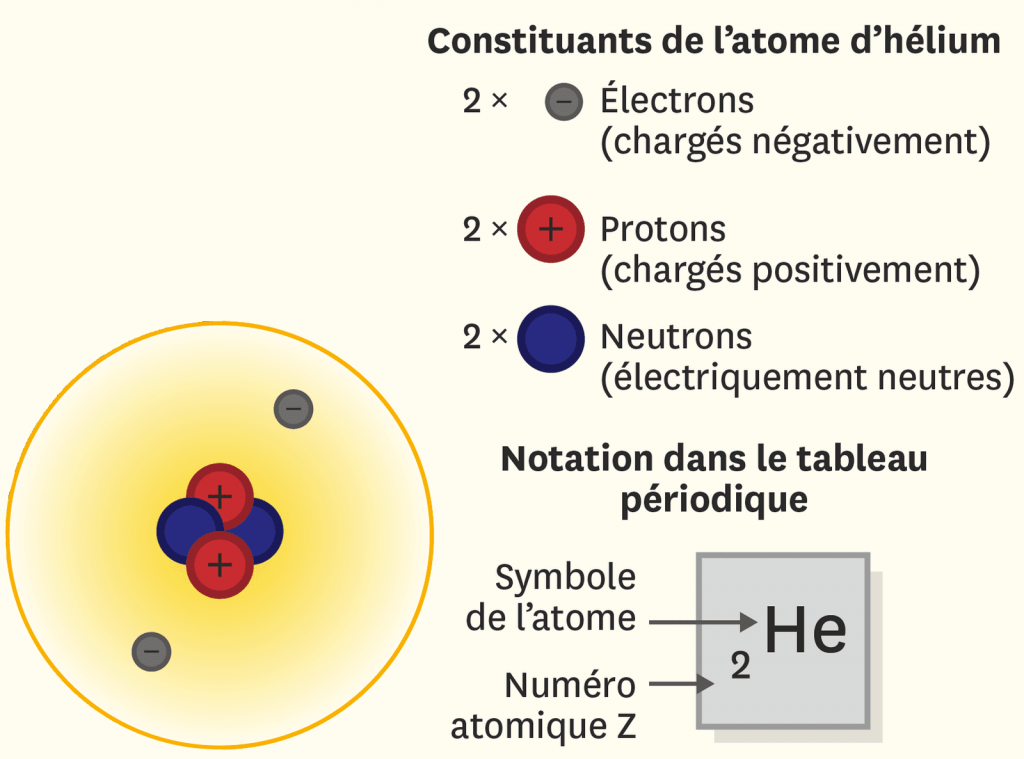
Vocabulaire :
charge électrique, nucléon, proton, neutron, électron, noyau, nuage électronique, numéro atomique
Activités
activités pour comprendre (en classe)
Activité 3 p.196
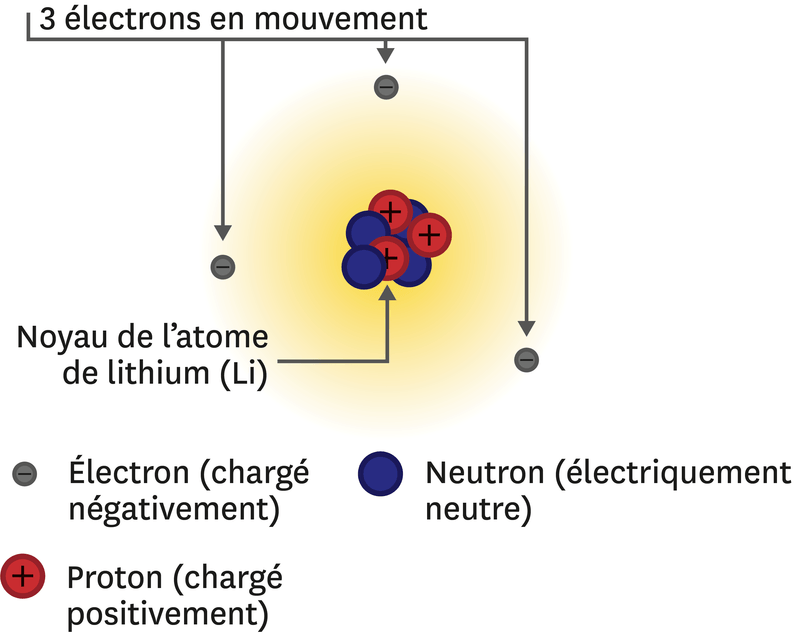
1) Particules constituant l’atome ci-contre : Les trois particules sont les protons et les neutrons qui forment le noyau de l’atome en son centre et les électrons qui sont en mouvement autour du noyau.
2) Particules constituant l’atome d’Hydrogène : ce sont forcément le proton (dans le rôle du noyau) et l’électron (en mouvement autour).
3) Que veut dire ‘ électriquement neutre’ ? Dans un atome le nombre d’électrons doit toujours être égal au nombre de protons afin que celui-ci soit électriquement neutre.
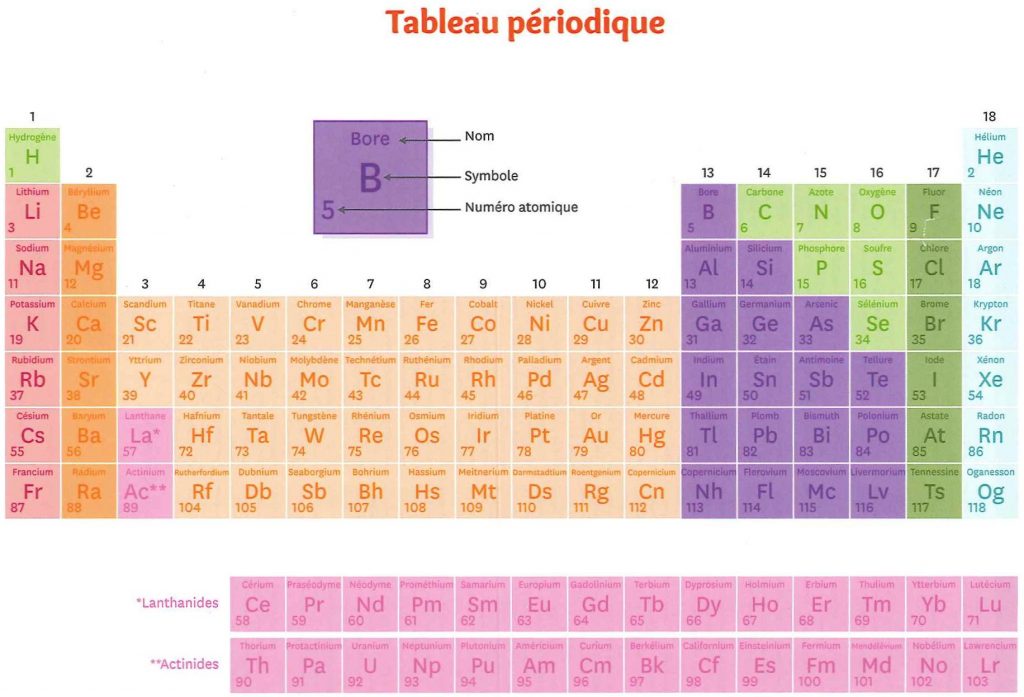
4) Quelles informations contient chaque case du tableau périodique ? Dans chaque case de la classification périodique, on trouve le symbole de l’atome. On trouve également le nombre de protons de l’atome, défini comme son numéro atomique et noté avec la lettre Z.
Exercices corrigé 7 p.201 et similaire 8 p.201
Ex. 7 p.201
1. Donne le nom et le symbole de l’atome qui a pour numéro atomique Z = 26
> L’atome qui a pour numéro atomique Z = 26 se trouve dans la 26e case du tableau périodique. Il s’agit du fer de symbole Fe.
2. Donne le nom et le symbole de l’atome qui a 7 protons dans son noyau.
> Par définition, le nombre de protons est le numéro atomique Z de l’atome. Ici, il s’agit de l’atome pour lequel Z = 7, soit d’après le tableau, de l’azote de symbole N.
3. Donne le nom et le symbole de l’atome qui possède 8 électrons.
> Par définition, le nombre de protons est le numéro atomique Z de l’atome. Ici, il s’agit de l’atome pour lequel Z = 7, soit d’après le tableau, de l’azote de symbole N.
Ex 8 p.201
1. Donne le nom et le symbole de l’atome qui a pour numéro atomique Z = 29.
> L’atome qui a pour numéro atomique Z = 29 est le cuivre (symbole : Cu).
2. Donne le nom et le symbole de l’atome qui a 79 protons dans son noyau.
> Un atome qui a 79 protons dans son noyau a pour numéro atomique Z = 79. Il s’agit de l’atome d’or (symbole : Au).
3. Donne le nom et le symbole de l’atome qui possède 47 électrons.
> Un atome qui possède 47 électrons possède aussi 47 protons puisqu’il est électriquement neutre. Il a donc pour numéro atomique Z = 47. Il s’agit de l’atome d’argent (symbole : Ag).
activités complémentaire
activités PCCL
- (35) Structure interne du noyau | protons – neutrons
- (31) Associer un élément et son numéro atomique
- (32) Reconnaître un élément | le situer dans le tableau périodique
fiche méthode

Applications
vérification des connaissances

à la maison


